작용기
덤프버전 :
분류
1. 개요[편집]
분자 내에서 비슷한 성질을 띠는 원자 그룹들을 묶어서 분류해놓은 것이다. 따라서 작용기(-基)는 간혹 원자단(原子團)이라고도 한다.
수소(H),산소(O),탄소(C)가 일단 기본 원자들이다.
2. 종류[편집]
한글명명법은 대한화학회 자료를 따름 대한화학회 화학술어집
2.1. 탄화수소 & 할로젠 계열[편집]
메틸기(methyl基,-group) -CH3의 작용기이다. 가장 간단한 알킬이며 비극성이다. 따라서 소수성을 띈다.
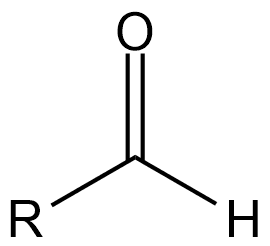
2.2. 카보닐기(Carbonyl) 계열[편집]
카보닐기는 탄소와 산소의 이중결합 구조(C=O)를 갖는 (극성) 작용기이다. 화학식은 -CO
2.3. 산소를 포함하는 작용기(카보닐 계열 제외)[편집]
특히 극성 작용기인 알코올 계통의 하이드록시기(-OH)가 잘 알려져 있다.
2.4. 질소를 포함하는 작용기[편집]
2.5. 그 외의 작용기[편집]
 이 문서의 내용 중 전체 또는 일부는 2023-12-15 10:19:01에 나무위키 작용기 문서에서 가져왔습니다.
이 문서의 내용 중 전체 또는 일부는 2023-12-15 10:19:01에 나무위키 작용기 문서에서 가져왔습니다.[1] RCOSR'이면 싸이오에스터(Thioester)[2] 중간에 S가 하나 더 들어가면 이황화물(Disulfide)[3] 구조가 한 번 더 반복되면 이인산염(Diphosphate)